Causas de la diabetes Mellitus tipo 2
-
Causas de la Diabetes Mellitus tipo 2

La resistencia a la insulina y la secreción anormal de ésta son aspectos centrales del desarrollo de DM de tipo 2. Aunque persisten las controversias en cuanto al defecto primario, en su mayor parte los estudios se inclinan a favor de que la resistencia a la insulina precede a los defectos de su secreción, y que la diabetes se desarrolla sólo si se torna inadecuada la secreción de insulina.
Consideraciones geneticas
La Diabetes Mellitus de tipo 2 posee un fuerte componente genético. Aunque todavía no se han identificado los genes principales que predisponen a este trastorno, está claro que se trata de una enfermedad poligénica y multifactorial. Diversos loci genéticos contribuyen a la vulnerabilidad, y factores ambientales como nutrición y actividad física regulan todavía más la expresión fenotípica de la enfermedad. La concordancia de la DM de tipo 2 en gemelos idénticos se sitúa entre 70 y 90%. Los individuos con un progenitor con DM de tipo 2 tienen más riesgo de diabetes; si ambos progenitores tienen Diabetes Mellitus de tipo 2, el riesgo en la descendencia puede alcanzar el 40%. En muchos familiares en primer grado no diabéticos de sujetos con Diabetes Mellitus de tipo 2 existe resistencia a la insulina, demostrada por una menor utilización de glucosa por el músculo esquelético. Sin embargo, la definición de las alteraciones genéticas de la Diabetes Mellitus de tipo 2 continúa siendo un reto, porque el defecto genético de la secreción o la acción de la insulina puede no manifestarse a menos que se superponga a un suceso ambiental u otro defecto genético, como la obesidad. Las mutaciones en varias moléculas que participan en la acción de la insulina (p. ej., receptor de la insulina y enzimas participantes en la homeostasia de la glucosa) explican una fracción muy pequeña de los casos de Diabetes Mellitus de tipo 2. De manera semejante, no se han encontrado defectos genéticos en las proteínas que participan en la secreción de insulina en la mayoría de los individuos que experimentan la diabetes de este tipo. Se está empleando el rastreo a toda la amplitud del genoma en busca de mutaciones o polimorfismos relacionados con la Diabetes Mellitus de tipo 2, en un esfuerzo por identificar los genes relacionados con esta forma de la enfermedad. En poblaciones hispanas y algunas otras se relaciona con este trastorno el gen de la proteasa calpaína 10.
Fisiopatología
La diabetes de tipo 2 se caracteriza por tres alteraciones fisiopatológicas: trastorno de la secreción de insulina, resistencia periférica a ésta y producción hepática excesiva de glucosa. La obesidad, en especial la visceral o central (como es evidente en el índice cintura-cadera), es muy frecuente en esta forma de diabetes. La resistencia a la insulina que acompaña a la obesidad aumenta la resistencia a la insulina determinada genéticamente de la DM de tipo 2. Los adipocitos secretan cierto número de productos biológicos (leptina, factor de necrosis tumoral alfa, ácidos grasos libres, resistina y adiponectina) que modulan la secreción de insulina, la acción de la insulina y el peso corporal, y pueden contribuir a la resistencia a la insulina. En las fases tempranas del trastorno, la tolerancia a la glucosa permanece normal, a pesar de la resistencia a la insulina, porque las células beta pancreáticas compensan aumentando la producción de insulina (fig. 323-6). A medida que avanzan la resistencia a la insulina y la hiperinsulinemia compensadora, los islotes pancreáticos se tornan incapaces de mantener el estado de hiperinsulinismo. Se desarrolla entonces IGT, caracterizado por grandes elevaciones de la glucemia posprandial. Cuando declina todavía más la secreción de insulina y aumenta la producción hepática de glucosa, aparece la diabetes manifiesta con hiperglucemia en ayuno. Finalmente ocurre el fallo de las células beta. A menudo están elevados los marcadores de la inflamación como IL-6 y proteína C reactiva en la diabetes de tipo 2.
Cambios metabólicos que ocurren el desarollo de la diabetes mellitus (DM) de tipo 2. Le secreción de insulina y la sensibilidad a ésta se encuentran relacionados, y conforme el individio se hace más resistente a esta hormona (al pasar del punto A al punto B) se incrementa su secreción. La incapacidad de compensar el problema mediante aumento de la secreción de insulina da por resulto, inicialmente, trastorno de la tolerancia a la glucosa (IGT, punto C) y en última instancia DM de tipo 2 (punto D).
Resistencia a la insulina
La capacidad disminuida de la insulina para actuar con eficacia sobre tejidos diana periféricos (en particular muscular y hepático) es un aspecto sobresaliente de la DM de tipo 2 y es resultado de una combinación de susceptibilidad genética y obesidad. La resistencia es relativa, porque los niveles supranormales de insulina circulante normalizarán la glucemia plasmática. Las curvas dosisrespuesta de la insulina muestran un desplazamiento hacia la derecha, que indica menor sensibilidad, y una respuesta máxima reducida, que refleja disminución global del empleo de glucosa (30 a 60% inferior al de los sujetos normales). La resistencia a la acción de la insulina altera la utilización de glucosa por los tejidos sensibles a insulina y aumenta la producción hepática de glucosa; ambos efectos contribuyen a la hiperglucemia de la diabetes. El aumento de la producción hepática de glucosa es responsable predominantemente de los elevados niveles de FPG, mientras que el decremento de la utilización periférica de glucosa produce hiperglucemia posprandial. En el músculo esquelético existe un trastorno mayor del uso no oxidativo de la glucosa (formación de glucógeno) que del metabolismo oxidativo de la glucosa por la glucólisis. La utilización de la glucosa por los tejidos independientes de la insulina no está alterada en la DM de tipo 2.
Todavía no se ha desentrañado el mecanismo molecular preciso de la resistencia a la insulina en la diabetes de tipo 2. Los niveles de receptor de insulina y de actividad de cinasa de tirosina están disminuidos, pero lo más probable es que estas alteraciones sean secundarias a la hiperinsulinemia y no un defecto primario. Por tanto, se cree que en la resistencia a la insulina el factor predominante son los defectos posteriores al receptor (fig. 323-4). Los polimorfismos del IRS-1 pueden asociarse a intolerancia a la glucosa, lo cual suscita la posibilidad de que se combinen polimorfismos en diversas moléculas posreceptor para crear el estado de resistencia a la insulina. En la actualidad la patogénesis de la resistencia a la insulina se investiga centrándose en un defecto de la señalización de la cinasa de PI-3, que reduce la transposición de GLUT4 a la membrana plasmática, entre otras anormalidades. Cabe insistir en que no todas las vías de transducción de las señales de la insulina son resistentes a los efectos de esta hormona [p. ej., las que controlan la multiplicación y la diferenciación celulares y emplean la vía de la cinasa de proteína activada por mitógenos (mitogen-activated protein, MAP); fig. 323-4]. Como consecuencia, la hiperinsulinemia puede incrementar la acción de la insulina a través de estas vías, lo que aceleraría en potencia los trastornos relacionados con la diabetes, como la ateroesclerosis.
Otra teoría planteada recientemente propone que pueden contribuir a la patogénesis de la DM de tipo 2 las concentraciones elevadas de ácidos grasos libres, aspecto frecuente en la obesidad. Los ácidos grasos libres pueden obstaculizar el empleo de glucosa por el músculo esquelético, promover la producción de este azúcar por el hígado y trastornar la función de la célula beta.
Trastorno de la secreción de insulina
La secreción de insulina y la sensibilidad a ella están relacionadas entre sí. En la Diabetes Mellitus de tipo 2, la secreción de insulina aumenta inicialmente en respuesta a la insulinorresistencia, con el fin de mantener una tolerancia normal a la glucosa. Al principio el defecto de la secreción de insulina es leve y afecta de manera selectiva la secreción de insulina estimulada por glucosa. La respuesta a otros secretagogos diferentes de la glucosa, como la arginina, está intacta. Finalmente, el defecto de la secreción de insulina avanza a un estado de secreción de insulina visiblemente inadecuada.
La razón (o razones) del declive de la capacidad secretoria de insulina en la Diabetes Mellitus de tipo 2 no están claras. A pesar de que se supone que un segundo defecto genético (superpuesto a la resistencia a insulina) lleva al fracaso de las células beta, hasta la fecha una intensa investigación genética ha excluido mutaciones en candidatos a genes de los islotes. El polipéptido amiloide de los islotes, o amilina, es cosecretado por la célula beta y probablemente forma el depósito de fibrillas amiloides que se encuentra en los islotes de diabéticos de tipo 2 de larga evolución. Se ignora si estos depósitos insulares de amiloide son un fenómeno primario o secundario. También el ambiente metabólico puede ejercer un efecto negativo sobre la función de los islotes. Por ejemplo, la hiperglucemia crónica altera de manera paradójica la función de los islotes (“toxicosis por glucosa”) y lleva a un empeoramiento de la hiperglucemia. La mejora del control de la glucemia se acompaña con frecuencia de un mejor funcionamiento insular. Además, la elevación de los valores de ácidos grasos libres (“lipotoxicosis”) también empeora el funcionamiento de los islotes.
Aumento de la producción hepática de glucosa
En la Diabetes Mellitus de tipo 2, la resistencia hepática a la insulina refleja la incapacidad de la hiperinsulinemia de suprimir la gluconeogénesis, lo que produce hiperglucemia en ayunas y disminución del almacenamiento de glucosa en el hígado en el período posprandial. El aumento de la producción hepática de glucosa ocurre en una fase temprana de la evolución de la diabetes, aunque probablemente es posterior al inicio de las alteraciones de la secreción insulínica y a la resistencia a la insulina en el músculo esquelético.
Síndromes de resistencia a la insulina
La resistencia a la insulina caracteriza a un espectro de trastornos, y entre ellos la hiperglucemia representa una de las características que se diagnostican con más facilidad. Síndrome metabólico,síndrome de resistencia a la insulina y síndrome X son términos empleados para describir una constelación de trastornos del metabolismo que incluye resistencia a la insulina, hipertensión, dislipidemia [concentración baja de lipoproteínas de alta densidad (high-density lipoprotein, HDL) y elevación de los triglicéridos], obesidad central o visceral, diabetes de tipo 2 o IGT con IFG, y enfermedad cardiovascular acelerada. Este síndrome es muy frecuente. Los Centers for Disease Control and Prevention (CDC) estiman que lo experimentan 20% de los adultos de Estados Unidos. Las pruebas epidemiológicas se inclinan a favor de la hiperinsulinemia como marcador del riesgo de arteriopatía coronaria, aunque no ha podido demostrarse una función etiológica del exceso de insulina.
Diversas formas relativamente raras de resistencia grave a la insulina abarcan características de la Diabetes Mellitus de tipo 2 o IGT (cuadro 323-1). Son también manifestaciones físicas frecuentes acantosis nigricans y signos de hiperandrogenismo (hirsutismo, acné y oligomenorrea en mujeres). Se han descrito en adultos dos síndromes definidos de resistencia grave a la insulina: 1) el tipo A, que afecta a mujeres jóvenes y se caracteriza por intensa hiperinsulinemia, obesidad y datos de hiperandrogenismo, y 2) el tipo B, que afecta a mujeres de mediana edad y se caracteriza por hiperinsulinemia intensa, datos de hiperandrogenismo y trastornos autoinmunitarios. Los individuos con el síndrome de resistencia a la insulina de tipo A tienen un defecto no precisado en la vía de señalización de la insulina; los pacientes con el tipo B poseen autoanticuerpos contra el receptor de insulina. Éstos pueden bloquear la unión de la insulina o estimular al receptor, provocando hipoglucemia intermitente.
El síndrome de ovario poliquístico (polycistic ovary syndrome, PCOS) es un trastorno frecuente que afecta a mujeres premenopáusicas y que se caracteriza por anovulación crónica e hiperandrogenismo (cap. 326). En una fracción considerable de las mujeres con PCOS se observa resistencia a la insulina, y el trastorno aumenta notablemente el riesgo de DM de tipo 2, con independencia de los efectos de la obesidad. Tanto la metformina como las tiazolidinadionas pueden atenuar la hiperinsulinemia, mejorar el hiperandrogenismo, inducir la ovulación y mejorar los valores de lípidos plasmáticos, pero no está aprobado su empleo para esta indicación.
Prevención
La DM de tipo 2 va precedida por un período de IGT, y diversas modificaciones del modo de vida así como varios agentes farmacológicos impiden o retrasan el inicio de esta enfermedad. El Diabetes Prevention Program (DPP) demostró que los cambios intensivos en el modo de vida (dieta y ejercicio durante 30 min/día cinco veces a la semana) de los individuos con IGT previno o retrasó el desarrollo de la diabetes de tipo 2 en 58% de los casos en comparación con lo ocurrido en el grupo de placebo. Este efecto se observó en todos los casos señalados independientemente de edad, sexo o grupo étnico. En el mismo estudio, la metformina previno o retrasó la diabetes en 31% de los casos en comparación con lo observado en el grupo de placebo. Los sujetos del grupo de intervención en el modo de vida perdieron 5 a 7% del peso corporal durante los tres años que duró el estudio. Los estudios efectuados en poblaciones finesas y chinas indicaron una eficacia semejante de la dieta y el ejercicio para prevenir o retrasar la DM de tipo 2; acarbosa, metformina y tiazolidinadionas tienen este mismo efecto, pero son medicaciones aún no aprobadas para esta finalidad. Cuando se administraron a individuos no diabéticos por otros motivos (cardíacos, reducción del colesterol, etc.), dos agentes farmacológicos (ramiprilo y pravastatina) redujeron el número de nuevos casos de diabetes. Los individuos con fuertes antecedentes familiares, quienes se encuentran en alto riesgo de desarrollar DM y las personas con IFG o IGT, deben ser alentados con firmeza para que conserven un índice de masa corporal (body mass index, BMI) normal y efectúen actividad física con regularidad.
Related posts:





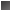





May 7th, 2011 at 8:05 pm
Basado en observaciones neuroquirurgicas,recientemente he publicado un articulo en la Rev Mex Cardiol 2011,22(1):39-43,en donde concluyo que la DM tipo 2 es causado por isquemia progresiva en el hipotàlamo anterior y luego en el pancreas endocrino.
Revisar dicho articulo