Complicaciones de la Diabetes
-
!-- CODIGO ADPV -->
Neuropatía y diabetes mellitus
Alrededor de 50% de los sujetos con Diabetes Mellitus de tipos 1 y 2 de larga evolución presentan neuropatía diabética.
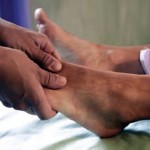 Puede manifestarse en forma de polineuropatía, mononeuropatía, neuropatía vegetativa (autónoma) o combinaciones de ellas. Como sucede con otras complicaciones de la DM, el desarrollo de neuropatía se correlaciona con la duración de la diabetes y con el control de la glucemia; ocurre pérdida de fibras nerviosas tanto mielínicas como amielínicas. Como los aspectos clínicos de la neuropatía diabética son semejantes a los de otras neuropatías, deberá considerarse acertado el diagnóstico de neuropatía diabética sólo después de haber excluido otros posibles aspectos etiológicos.
Puede manifestarse en forma de polineuropatía, mononeuropatía, neuropatía vegetativa (autónoma) o combinaciones de ellas. Como sucede con otras complicaciones de la DM, el desarrollo de neuropatía se correlaciona con la duración de la diabetes y con el control de la glucemia; ocurre pérdida de fibras nerviosas tanto mielínicas como amielínicas. Como los aspectos clínicos de la neuropatía diabética son semejantes a los de otras neuropatías, deberá considerarse acertado el diagnóstico de neuropatía diabética sólo después de haber excluido otros posibles aspectos etiológicos.Polineuropatía y mononeuropatía
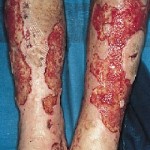 La forma más frecuente de neuropatía diabética es la polineuropatía simétrica distal. Se presenta con frecuencia máxima como pérdida de la sensibilidad distal. También ocurren hiperestesias, parestesias y disestesias. Puede desarrollarse cualquier combinación de estos síntomas conforme avanza la neuropatía. Los síntomas consisten en sensación de adormecimiento, hormigueo, pinchazos o ardor quemante que se inicia en los pies y se extiende en sentido proximal. En algunos de estos individuos sobreviene dolor neuropático precedido, ocasionalmente, por mejoría de su control de la glucemia. El dolor afecta de manera característica las extremidades inferiores, suele percibirse en reposo y empeora durante la noche. Se han descrito formas tanto aguda (que dura menos de 12 meses) como crónica de la neuropatía diabética dolorosa. Conforme avanza este trastorno neurológico, el dolor va cediendo y acaba por desaparecer, pero persiste un déficit de la sensibilidad en las extremidades inferiores. La exploración física descubre pérdida de la sensibilidad, pérdida del reflejo del tobillo y sentido de la posición anormal.
La forma más frecuente de neuropatía diabética es la polineuropatía simétrica distal. Se presenta con frecuencia máxima como pérdida de la sensibilidad distal. También ocurren hiperestesias, parestesias y disestesias. Puede desarrollarse cualquier combinación de estos síntomas conforme avanza la neuropatía. Los síntomas consisten en sensación de adormecimiento, hormigueo, pinchazos o ardor quemante que se inicia en los pies y se extiende en sentido proximal. En algunos de estos individuos sobreviene dolor neuropático precedido, ocasionalmente, por mejoría de su control de la glucemia. El dolor afecta de manera característica las extremidades inferiores, suele percibirse en reposo y empeora durante la noche. Se han descrito formas tanto aguda (que dura menos de 12 meses) como crónica de la neuropatía diabética dolorosa. Conforme avanza este trastorno neurológico, el dolor va cediendo y acaba por desaparecer, pero persiste un déficit de la sensibilidad en las extremidades inferiores. La exploración física descubre pérdida de la sensibilidad, pérdida del reflejo del tobillo y sentido de la posición anormal.La polirradiculopatía diabética es un síndrome caracterizado por dolor incapacitante situado en el territorio de distribución de una o más raíces nerviosas. Puede ir acompañado de debilidad motora. La radiculopatía intercostal o de tronco provoca dolor en el tórax o abdomen. La afección del plexo lumbar o el nervio femoral puede causar dolor en el muslo o la cadera y acompañarse de debilidad motora en los flexores o extensores de la cadera (amiotrofia diabética). Por fortuna, las polirradiculopatías diabéticas suelen resolverse espontáneamente en seis a 12 meses.
La mononeuropatía (disfunción de nervios craneales o periféricos aislados) es menos frecuente que la polineuropatía en la DM y se presenta en forma de dolor o debilidad motora en el territorio de un solo nervio. Se ha propuesto una etiología vascular, pero se ignora su patogenia. Lo más frecuente es la afección del tercer par craneal, y la diplopía anuncia su presencia. La exploración física revela ptosis y oftalmoplejía, con miosis normal a la luz. A veces se afectan los pares craneales IV, VI o VII (parálisis de Bell). También puede haber mononeuropatías periféricas o afección simultánea de más de un nervio (mononeuropatía múltiple).
Neuropatía vegetativa (autónoma)
Los pacientes con DM de tipo 1 o 2 de larga evolución pueden presentar signos de disfunción vegetativa que afectan los sistemas colinérgico, noradrenérgico y peptidérgico (péptidos como polipéptido pancreático, sustancia P, etc.). Es posible que la neuropatía vegetativa relacionada con la DM afecte numerosos aparatos y sistemas, como el cardiovascular, el digestivo, el genitourinario, el seudomotor y el metabólico. Las neuropatías vegetativas que afectan al aparato cardiovascular tienen el potencial de provocar taquicardia de reposo e hipotensión ortostática. También se han atribuido a la neuropatía autónoma casos de muerte repentina. Es probable que la gastroparesia y las dificultades de vaciamiento de la vejiga estén relacionadas con la neuropatía vegetativa de la Diabetes Mellitus (véase más adelante en este capítulo). La disfunción del sistema nervioso simpático puede producir hiperhidrosis de las extremidades superiores y anhidrosis de las inferiores. En este último caso es posible que ocurran sequedad de piel y grietas, de modo que aumenta el riesgo de úlceras en los pies. La neuropatía autónoma puede reducir la liberación de hormonas de la contrarregulación, lo que conlleva incapacidad para detectar adecuadamente la hipoglucemia (hipoglucemia inadvertida; cap. 324), por lo cual el paciente queda expuesto a un riesgo de hipoglucemia grave y se complican los esfuerzos por lograr un mejor control glucémico.
Tratamiento
El tratamiento de la neuropatía diabética dista de ser satisfactorio. Se debe perseguir un mejor control de la glucemia, que mejorará la velocidad de conducción nerviosa, pero no necesariamente los síntomas de neuropatía diabética. Los intentos de mejorar el control de la glucemia pueden complicarse por efecto de la neuropatía vegetativa y la hipoglucemia inadvertida. La clave del tratamiento es evitar las neurotoxinas (alcohol), administrar suplementos vitamínicos contra posibles deficiencias (B12, B6, folato; cap. 61), y dar apoyo sintomático. En la actualidad, los inhibidores de la reductasa de aldosa no ofrecen alivio sintomático importante. La pérdida de sensibilidad en el pie pone al paciente en peligro de ulceración y de sus secuelas; por ello reviste importancia capital la prevención de estos problemas. Como el dolor de la neuropatía diabética puede resolverse en el transcurso del primer año, es posible suspender los analgésicos a medida que se produce el daño neuronal progresivo. La neuropatía diabética dolorosa crónica es difícil de tratar pero puede responder a antidepresivos tricíclicos (amitriptilina, desipramina, nortriptilina), gabapentina, antiinflamatorios no esteroideos (deben evitarse si existe disfunción renal), y otros agentes (mexilitina, fenitoína, carbamazepina, crema de capsaicina). Tal vez sea necesario referir a un centro de tratamiento del dolor.
El tratamiento de la hipotensión ortostática secundaria a la neuropatía vegetativa es difícil. Diversos fármacos producen beneficios limitados (fludrocortisona, midodrina, clonidina, octreótido y yohimbina) pero tienen efectos secundarios importantes. Las maniobras no farmacológicas (ingerir cantidades adecuadas de sal, evitar la deshidratación y los diuréticos, usar medias de compresión) pueden proporcionar algún beneficio.
Disfunción gastrointestinal o genitourinaria
La DM de larga evolución de los tipos 1 y 2 puede afectar la motilidad y el funcionamiento del tubo digestivo y el aparato genitourinario. Los síntomas digestivos más destacados son retraso del vaciamiento gástrico (gastroparesia) y alteraciones de la motilidad del intestino delgado y el grueso (estreñimiento o diarrea). La gastroparesia puede presentarse con síntomas de anorexia, náuseas, vómitos, saciedad precoz y distensión del abdomen. La gammagrafía tras la ingestión de una comida marcada con un radiotrazador es la forma óptima de demostrar el retraso del vaciamiento gástrico, pero se están desarrollando “pruebas de aliento” no invasoras tras la ingestión de una comida marcada con radioisótopo. Aunque la disfunción parasimpática secundaria a la hiperglucemia crónica es importante en el desarrollo de la gastroparesia, la propia hiperglucemia altera el vaciamiento gástrico. Una característica frecuente de la neuropatía vegetativa digestiva relacionada con la DM es la diarrea nocturna, que alterna con estreñimiento. En la DM de tipo 1 estos síntomas deben suscitar la búsqueda de enfermedad celíaca, por su mayor frecuencia. En la diabetes de larga evolución es frecuente la disfunción esofágica, pero suele ser asintomática.
La neuropatía autónoma diabética puede provocar afecciones genitourinarias que comprenden cistopatía, disfunción eréctil y disfunción sexual femenina (descenso del deseo sexual, dispareunia, decremento de la lubricación vaginal). Los síntomas de la cistopatía empiezan por la incapacidad para sentir el llenado vesical y realizar una micción completa. A medida que empeora la contractilidad vesical, aumenta la capacidad de la vejiga y el residuo posmiccional, lo que produce síntomas de dificultad para iniciar la micción, decremento de la frecuencia miccional, incontinencia e infecciones urinarias repetidas. La valoración diagnóstica comprende cistometría y estudios urodinámicos.
La disfunción eréctil y la eyaculación retrógrada son muy frecuentes en la DM y pueden ser de los primeros indicios de neuropatía diabética (cap. 43). La disfunción eréctil, cuya frecuencia aumenta con la edad del paciente y la duración de la diabetes, puede ocurrir en ausencia de otros signos de neuropatía vegetativa diabética.
Tratamiento
Los tratamientos actuales de estas complicaciones de la DM son insatisfactorios. Un objetivo fundamental debería ser elevar el control de la glucemia, porque algunos aspectos (neuropatía, función gástrica) pueden mejorar. Las comidas pequeñas y frecuentes, más fáciles de digerir (líquidas) y de bajo contenido en grasa y fibra pueden reducir al mínimo los síntomas de gastroparesia. Probablemente la cisaprida (10 a 20 mg antes de cada comida) es el fármaco más eficaz, pero ha sido retirada del mercado estadounidense salvo para circunstancias especiales. Otros fármacos con alguna eficacia son los agonistas de la dopamina (metoclopramida, 5 a 10 mg, y domperidona, 10 a 20 mg antes de cada comida), y el betanecol (10 a 20 mg antes de cada comida). La eritromicina interactúa con el receptor de la motilina y puede promover el vaciamiento gástrico. La diarrea diabética sin proliferación bacteriana se trata de manera sintomática con loperamida pero puede responder a la clonidina en dosis altas (0.6 mg tres veces al día) o el octreótido (50 a 75 g tres veces al día por vía subcutánea). A veces resulta útil tratar la proliferación bacteriana con antibióticos.
La cistopatía diabética se debe tratar con horario de micción o autosondaje. Los medicamentos, como el betanecol, tienen eficacia inconstante. El fármaco de elección para la disfunción eréctil es el sildenafil, pero la eficacia en los diabéticos es ligeramente inferior que en los no diabéticos. La disfunción sexual en las mujeres puede mejorar con el empleo de lubricantes vaginales, el tratamiento de las infecciones vaginales y reposición hormonal local o general con estrógenos.
Morbilidad y mortalidad cardiovasculares
La incidencia de enfermedades cardiovasculares está incrementada en quienes experimentan DM de tipos 1 y 2. El Framingham Heart Study reveló un incremento notable de arteriopatía periférica, insuficiencia cardíaca congestiva, arteriopatía coronaria, infarto del miocardio (myocardial infarction, MI) y muerte repentina (incremento del riesgo de una a cinco veces) en la DM. La American Heart Association definió recientemente a la diabetes mellitus como factor mayor de riesgo de enfermedad cardiovascular (la colocó en la misma categoría que tabaquismo, hipertensión e hiperlipidemia). Los pacientes con diabetes de tipo 2 sin MI previo experimentan un riesgo semejante de enfermedad cardiovascular y sucesos relacionados que los sujetos no diabéticos que han sufrido de antemano un infarto del miocardio. A causa de la prevalencia extremadamente elevada de enfermedad cardiovascular subyacente en los individuos diabéticos (en particular con DM de tipo 2), deben buscarse manifestaciones de enfermedad vascular ateroesclerótica en el enfermo diabético que tiene síntomas sugerentes de isquemia cardíaca, arteriopatía periférica o carotídea o electrocardiograma en reposo que indica MI previo, o que planea iniciar un programa de ejercicios, experimenta proteinuria o tiene otros dos factores de riesgo cardíaco (recomendaciones de la ADA). Es frecuente la ausencia de dolor torácico (“isquemia silenciosa”) en los diabéticos, y está indicada la valoración cardíaca concienzuda en los que se someterán a una operación quirúrgica mayor. El pronóstico para los individuos diabéticos que experimentan una arteriopatía coronaria o un infarto del miocardio es peor que en quienes no son diabéticos. Es más probable que la enfermedad arterial coronaria abarque muchos vasos en los individuos con diabetes mellitus.
El incremento de la morbilidad y la mortalidad cardiovasculares parece relacionarse con la sinergia de la hiperglucemia con otros factores de riesgo cardiovascular. Por ejemplo, después de controlar todos los factores de riesgo cardiovascular conocidos, la DM de tipo 2 aumenta al doble la mortalidad cardiovascular en los varones y al cuádruplo en las mujeres. Los factores de riesgo de macroangiopatía en los diabéticos son dislipidemia, hipertensión, obesidad, actividad física escasa y tabaquismo. Otros factores de riesgo específicos de la población diabética son oligoalbuminuria, macroproteinuria, elevación de la creatinina sérica y alteración de la función plaquetaria. La resistencia a la insulina, reflejada por aumento de los valores de insulina sérica, se asocia a un incremento del riesgo de complicaciones cardiovasculares tanto en diabéticos como en no diabéticos. Los individuos con resistencia a la insulina y DM de tipo 2 tienen valores elevados de inhibidores del activador del plasminógeno (especialmente de PAI-1) y de fibrinógeno, lo cual facilita la coagulación y trastorna la fibrinólisis, favoreciendo así el desarrollo de trombosis. La diabetes se acompaña también de disfunción endotelial, del músculo liso vascular y plaquetaria.
Se carece de pruebas de que un mejor control de la glucemia reduzca las complicaciones cardiovasculares en la DM; de hecho, es posible que las complicaciones macrovasculares queden sin modificar o incluso empeoren con dicho tratamiento. Persiste la preocupación respecto al efecto anabólico y aterógeno de la insulina, porque en los no diabéticos los valores séricos más altos de insulina (que indican resistencia a ésta) se asocian a mayor riesgo de morbimortalidad cardiovascular. En el DCCT, el número de acontecimientos cardiovasculares no mostró diferencias entre los grupos de tratamiento intensivo y ordinario. Sin embargo, la duración de la diabetes en estos sujetos era relativamente corta, y el número total de sucesos fue muy bajo. La mejora del perfil lipídico de los sujetos en tratamiento intensivo [colesterol total y colesterol de las lipoproteínas de baja ensidad (low-density lipoprotein, LDL) más bajos y triglicéridos más bajos] sugirió que el tratamiento intensivo puede reducir el riesgo de morbilidad y mortalidad cardiovascular asociado a la DM. En el UKPDS, la ejoría del control glucémico no redujo de manera concluyente la mortalidad cardiovascular. Es importante el echo de que el tratamiento con insulina y con sulfonilureas no pareció aumentar el riesgo de enfermedad ardiovascular en los sujetos con DM de tipo 2, lo que refuta las afirmaciones anteriores de que estas ustancias tienen potencial aterógeno.
Además de la coronariopatía isquémica, en los diabéticos existe incremento de la enfermedad vascular cerebral (aumento de tres veces en la frecuencia de apoplejía). Los sujetos con DM tienen más riesgo de insuficiencia cardíaca congestiva (miocardiopatía diabética). Probablemente la causa de este trastorno es multifactorial e incluye factores como isquemia miocárdica por ateroesclerosis, hipertensión y disfunción de los miocardiocitos secundaria a hiperglucemia crónica.
Tratamiento
En general, el tratamiento de la cardiopatía isquémica no es distinto en los diabéticos (cap. 226). Los procedimientos de revascularización para la cardiopatía isquémica, como la intervención coronaria percutánea (percutaneous coronary interventions, PCI) y la cirugía de derivación coronaria con injerto (coronary artery, CABG) son menos eficaces en los diabéticos. La tasa inicial de éxito con la PCI es similar en bypass grafting diabéticos y no diabéticos, pero en éstos la frecuencia de reestenosis es mayor, y tanto la permeabilidad a largo plazo como los índices de supervivencia son inferiores. El empleo de endoprótesis vasculares y un inhibidor del receptor plaquetario GPIIb/IIIa ha mejorado los resultados en los pacientes diabéticos. En caso de DM no se altera la mortalidad perioperatoria por CABG, pero se reduce la supervivencia tanto a corto como a largo plazos. Ensayos clínicos recientes indican que los diabéticos con enfermedad coronaria de muchos vasos o que han sufrido recientemente un infarto de miocardio con onda Q tienen mejor supervivencia a largo plazo con CABG que con intervención coronaria percutánea.
La ADA ha insistido en la importancia del control de la glucemia y la modificación enérgica del riesgo cardiovascular en todas las personas que experimentan DM. La gran ansiedad que despertó el empleo de los antiadrenérgicos beta para tratar a los individuos diabéticos no debe impedir el empleo de estos agentes, puesto que benefician sin duda alguna a los pacientes con diabetes que han sufrido un MI. Pueden ser también particularmente beneficiosos los inhibidores de la ACE, y deberá pensarse en la conveniencia de administrarlos a enfermos con Diabetes Mellitus de tipo 2 y otros trastornos de riesgo (tabaquismo, dislipidemia, antecedentes de enfermedad cardiovascular, oligoalbuminuria).
El tratamiento antiplaquetario disminuye los acontecimientos cardiovasculares en los diabéticos con cardiopatía isquémica. Las recomendaciones actuales de la ADA sugieren el empleo de ácido acetilsalicílico como método de prevención secundaria de otros acontecimientos coronarios. Aunque no se dispone de datos que demuestren la eficacia en la prevención primaria de los acontecimientos coronarios, se debe considerar el tratamiento antiplaquetario, en especial en los diabéticos con otros factores de riesgo de cardiopatía isquémica como hipertensión, tabaquismo o dislipidemia. La dosis de ácido acetilsalicílico (81 a 325 mg) es la misma que en los no diabéticos. El tratamiento con este fármaco carece de efectos perjudiciales sobre la función renal o la hipertensión, y no afecta a la evolución de la retinopatía o la maculopatía diabéticas.



Comentarios