Cáncer testicular
-
Cáncer testicular
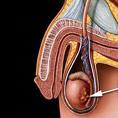 Los tumores primarios de células germinales (germ cell tumors, GCT) del testículo se deben a la transformación maligna de las células germinales primordiales y constituyen 95% de todas las neoplasias testiculares. Con escasa frecuencia, los GCT se forman fuera de las gónadas; por ejemplo, en el mediastino, el retroperitoneo y, muy rara vez, en la glándula pineal. Esta entidad se caracteriza por afectar a personas muy jóvenes, por la capacidad totipotencial para diferenciarse que tienen las células tumorales y por sus posibilidades de curación; alrededor de 95% de todos los pacientes recién diagnosticados pueden curarse. La experiencia adquirida en el tratamiento de los GCT se ha traducido en un pronóstico mejor.
Los tumores primarios de células germinales (germ cell tumors, GCT) del testículo se deben a la transformación maligna de las células germinales primordiales y constituyen 95% de todas las neoplasias testiculares. Con escasa frecuencia, los GCT se forman fuera de las gónadas; por ejemplo, en el mediastino, el retroperitoneo y, muy rara vez, en la glándula pineal. Esta entidad se caracteriza por afectar a personas muy jóvenes, por la capacidad totipotencial para diferenciarse que tienen las células tumorales y por sus posibilidades de curación; alrededor de 95% de todos los pacientes recién diagnosticados pueden curarse. La experiencia adquirida en el tratamiento de los GCT se ha traducido en un pronóstico mejor.Incidencia y epidemiología
En el año 2004 se diagnosticaron en Estados Unidos unos 9 000 casos nuevos de GCT testicular; la incidencia de esta neoplasia maligna se ha ido elevando lentamente en los últimos 40 años. Se observa con mayor frecuencia entre los 20 y 40 años de edad. La aparición de una tumoración testicular en un varón 50 o más años debe considerarse linfoma mientras no se demuestre lo contrario. El GCT es por lo menos cuatro o cinco veces más frecuente en los varones estadounidenses de ascendencia africana, y se ha observado una incidencia mayor en los países escandinavos y en Nueva Zelanda que en Estados Unidos.
Etiología y genética
La criptorquidia se asocia a un riesgo siete veces mayor de padecer un GCT. Los testículos criptorquídicos situados en el abdomen presentan mayor riesgo que los testículos inguinales. La orquiopexia debe realizarse antes de la pubertad, siempre que sea posible. La orquiopexia precoz disminuye el riesgo de GCT y aumenta la probabilidad de salvar el testículo. Cuando resulta imposible colocar un testículo criptorquídico en el escroto, se le debe extirpar. En cerca de 2% de los varones con GCT en un testículo aparece un nuevo tumor primario en el otro testículo. Los síndromes de feminización testicular elevan el riesgo de aparición de GCT, y el síndrome de Klinefelter se vincula con GCT del mediastino.
Un isocromosoma del brazo corto del cromosoma 12 [i(12p)] es patognomónico del GCT en todos los tipos histológicos. En casi todos los GCT existe un número excesivo de copias de 12p, bien en forma de i(12p), bien como un aumento de 12p en cromosomas con bandeo aberrante, pero el gen o los genes en 12p responsables de la patogenia aún no se han definido.
Manifestaciones clínicas
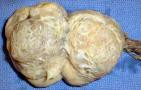 La aparición de una tumoración testicular indolora es un signo patognomónico de neoplasia testicular. Es más frecuente que los pacientes consulten por molestias o inflamación testicular compatibles con epididimitis u orquitis. En esas circunstancias, es razonable probar un ciclo de antibióticos. Pero si los síntomas perduran o sigue existiendo alguna anomalía residual, está indicado efectuar un examen ecográfico testicular.
La aparición de una tumoración testicular indolora es un signo patognomónico de neoplasia testicular. Es más frecuente que los pacientes consulten por molestias o inflamación testicular compatibles con epididimitis u orquitis. En esas circunstancias, es razonable probar un ciclo de antibióticos. Pero si los síntomas perduran o sigue existiendo alguna anomalía residual, está indicado efectuar un examen ecográfico testicular.La ecografía testicular está indicada siempre que se piensa en una neoplasia maligna del testículo y en casos de tumefacción testicular persistente o dolorosa. Si se detecta una tumoración testicular, debe realizarse una orquiectomía inguinal radical. Como el testículo se origina en la cresta gonadal de la cavidad peritoneal, sus vasos sanguíneos y su drenaje linfático proceden del abdomen y descienden junto con el testículo hasta el escroto. Se utiliza un acceso quirúrgico abdominal para no dejar brechas abiertas en las barreras anatómicas por donde las células tumorales se puedan diseminar.
Las metástasis retroperitoneales producen con frecuencia dolores de espalda que deben distinguirse del dolor debido a procesos musculoesqueléticos. Es rara la disnea secundaria a metástasis pulmonares. Los pacientes con niveles séricos altos de gonadotropina coriónica humana (human chorionic gonadotropin, hCG) consultan a veces por ginecomastia. Cuando el diagnóstico se retrasa, el proceso alcanza un estadio más avanzado y es posible entonces que disminuya la supervivencia.
La estadificación de los GCT comprende la medición de los niveles séricos de -fetoproteína (alpha-fetoprotein, AFP), hCG y deshidrogenasa láctica (lactate, LDH). Después de la orquiectomía deben realizarse una dehydrogenase radiografía de tórax y una tomografía computadorizada (computed tomography, CT) del abdomen y la pelvis. Si se sospecha la presencia de nódulos pulmonares, o afección mediastínica o de los hilios pulmonares se necesita además una CT del tórax. El estadio I se caracteriza porque el proceso tumoral se circunscribe al testículo, al epidídimo o al cordón espermático. En el estadio II el tumor ha alcanzado los ganglios linfáticos retroperitoneales (regionales). En el estadio III el proceso ha rebasado el retroperitoneo y afecta a los ganglios o las vísceras supradiafragmáticas. La estadificación puede ser “clínica” (basada únicamente en la exploración física, la medición de los marcadores sanguíneos y las radiografías) o “anatomopatológica”, apoyada en alguna técnica quirúrgica.
Los ganglios linfáticos regionales que drenan el testículo se encuentran en el retroperitoneo y los vasos sanguíneos proceden de los grandes vasos (para el testículo derecho) o de los vasos renales (para el testículo izquierdo). Debido a esto, los ganglios linfáticos que se afectan en primer lugar cuando aparece un tumor testicular del lado derecho son los ganglios intercavoaórticos situados inmediatamente por debajo de los vasos renales. En el caso de un tumor testicular izquierdo, los primeros ganglios linfáticos que se afectan están por fuera de la aorta (paraaórticos) y por debajo de los vasos renales izquierdos. En ambos casos, la diseminación tumoral hacia otros ganglios se dirige hacia abajo y hacia el lado opuesto y, con menos frecuencia, por encima del hilio renal. La participación ganglionar puede extenderse en dirección cefálica hacia los ganglios retrocrurales, mediastínicos posteriores y supraclaviculares. El tratamiento depende de la histología (seminomas o tumores no seminomatosos) y del estadio clínico del tumor.
IA
Testículos únicamente, sin
invasión vascular ni linfática (T1)IB
estículos únicamente,
con invasión vascular/
linfática (T2) o extensión
a través de la túnica
albugínea (T2) o afección
del cordón espermático
(T3) o del escroto (T4)IIA
Ganglios <2 cmIIB
Ganglios 2 a 5 cmIIC
Ganglios >5 cmIII
Metástasis a distanciaAnatomía patológica
Los GCT pueden ser seminomatosos o tumores no seminomatosos. Estos últimos son los más frecuentes en el tercer decenio de la vida y pueden mostrar todo el espectro de la diferenciación celular embrionaria y del adulto. Este proceso comprende cuatro tipos histológicos: carcinoma embrionario, teratoma, coriocarcinoma y tumor del saco vitelino (tumor del seno endodérmico). El coriocarcinoma, formado por citotrofoblastos y sincitiotrofoblastos, corresponde a una diferenciación trofoblástica maligna y se acompaña constantemente de secreción de hCG. El tumor del saco vitelino es la contrapartida maligna del saco vitelino fetal y conlleva secreción de AFP. El carcinoma embrionario puro puede secretar AFP, hCG, o ambas sustancias; este comportamiento es una prueba bioquímica de la diferenciación. El teratoma está formado por células de tipo somático procedentes de dos o más hojas germinales (ectodermo, mesodermo o endodermo). Cada una de estas variedades histológicas puede presentarse en forma aislada o combinada con las otras. Los GCT no seminomatosos tienen tendencia a dar metástasis precozmente en ciertas localizaciones, como los ganglios retroperitoneales y el parénquima pulmonar. Cerca de 33% de los pacientes acuden al médico con tumores circunscritos al testículo (estadio I), otro tercio con metástasis retroperitoneales (estadio II) y el tercio restante presenta ya metástasis extensas en los ganglios linfáticos o las vísceras situadas por encima del diafragma (estadio III).
El seminoma constituye aproximadamente 50% de todos los GCT, la mediana de la edad afectada es el cuarto decenio y, en general, tiene una evolución clínica más insidiosa. La mayoría de los pacientes (70%) consulta durante el estadio I del proceso, aproximadamente 20% lo hace en el estadio II, y 10% en el estadio III; son raras las metástasis pulmonares o en otras vísceras. La radioterapia es el tratamiento preferente en los pacientes cuyo proceso se encuentra en los estadios I y II, cuando los ganglios tienen <5 cm de diámetro máximo. Cuando el tumor contiene elementos seminomatosos y no seminomatosos, el tratamiento debe dirigirse contra el componente no seminomatoso, que es el más agresivo.
Marcadores tumorales
Para tratar a los pacientes con GCT resulta esencial realizar una vigilancia cuidadosa de los marcadores tumorales en el suero AFP y hCG, dada su importancia para el diagnóstico, como indicadores pronósticos, para controlar la respuesta al tratamiento y para detectar con anticipación una recidiva. Alrededor de 70% de los pacientes que consultan con un GCT no seminomatoso diseminado tiene concentraciones séricas altas de AFP, de hCG, o de ambos marcadores. Si bien la concentración de hCG puede estar alta en los pacientes con seminomas y con tumores no seminomatosos, la AFP aumenta sólo en los pacientes con tumores no seminomatosos. El dato de un nivel alto de AFP en un paciente con un tumor exclusivamente seminomatoso indica que existe un componente no seminomatoso oculto, y que el paciente debe tratarse de acuerdo con las normas del GCT no seminomatoso. El nivel de deshidrogenasa láctica (LDH) no es tan específico como la AFP o la hCG. Los niveles de LDH están elevados en 50 a 60% de los casos de tumores no seminomatosos metastásicos y hasta en 80% de los casos de seminomas avanzados.
Antes y después de la orquiectomía deben medirse los niveles de AFP, hCG y LDH. Las concentraciones altas de AFP y hCG descienden de acuerdo con una cinética de primer grado; la vida media de la hCG es de 24 a 36 h, y la de la AFP de cinco a siete días. Estos dos marcadores deben analizarse de manera seriada durante y después del tratamiento. Si se observa que cualquiera de estos marcadores o los dos vuelven a elevarse o no descienden de acuerdo con la vida media prevista, hay que pensar en la persistencia o en la recidiva del tumor.
No hay articulos relacionados.












November 10th, 2008 at 11:17 am
Buenas. Ante todo un cordial saludo. No soy médico, soy ingeniero, higienista ocupacional. Tengo la siguiente inquietud: ¿El cancer testicular puede ser de origen ocupacional? ¿Hay estudios al respecto? ¿Qué tipo de procesos podrían incidir en su aparición? Gracias.
August 14th, 2009 at 7:40 pm
Hasta la fecha el mayor riesgo comprobado lo tienen los pacientes con criptorquidia (testiculos no descendidos), ocupacional no hay ni siquiera sugerencias, se considera (sobretodo para los tumores de células germinales) que hay alteraciones en los cromosomas, principalmente el brazo corto del cromosoma 12 que se duplica y forma el isocromosoma 12p,y alteraciones el el gen DAD-R, y enfermedades de inmadurez de los testiculos, se ha visto que de ahi derivan. Otros que no comprobados son la expocisión a estrogenos y dietilestilbestrol antes de nacer, la vasectomia, la atrofia, y hasta la falta de leche materna pero solo los tres primeros estan asociados, asi que no se menciona riesgo ocupacional.
September 15th, 2009 at 3:35 am
porque un paciente con neoplasia de testiculo, manifiesta, obnubilacion, disartria y hemiparesa de un lada del cuerpo
December 3rd, 2009 at 5:17 pm
presento una bola dura con dolor sobre testiculo derecho que podra ser,
February 24th, 2010 at 9:59 pm
En el caso de un tumor testicular izquierdo, los primeros ganglios linfáticos que se afectan están por fuera de la aorta (paraaórticos) y por debajo de los vasos renales izquierdos. ¿Esto sucede siempre? ¿puede haber excepciones en un paciente de 19 años con tumor de células germinales?
puede ser que todo quede perfecto con la cirugía según el Dr. se detectó a tiempo, sin embargo, despues dijo que era seguro que el tumor siguiera una trayectoria igual a la que describen hacia la aorta. En el caso que el paciente presente esa trayectoria la cirugía que sigue sería la última es decir ya no habrá más metástasis que pronóstico tiene en caso de presentar la metástasis hacia la aorta, o bien a los ganglios linfáticos.
December 31st, 2010 at 11:23 am
tengo un mar de dudas, estoy recien asumiendo mi enfermedad, me detectaron cancer testicular (testiculo izquiedo), esto fue detectado el dia 20 y el dia 22 me estirparon el testiculo, el resultado de la biopcia señala lo siguiente.
tipo histologico……… tumor mixto de celulas germinales, constituido por 80 a 90% de carcionoma embrionario. 5 a 10% de seminoma.
tamaño……………… 32 cm
nivel de invacion……. limitado al testiculo
infiltracion vascular… Positiba, linfatica (T2).
Compromiso epididimo….. negativo.
Compromiso de cordon…… negativo.
testiculo adyacente……. neoplasia intratubular multifocal.
Bordes quirurgicos……… negativos.
NOTA, hay focos sospechosos de tumor del seno endodermico y de coriocarcinoma, por lo que se recomienda correlacion clinica y de marcadodes turmorales. Si la evalucion clinica lo estima necesario, se puede complementar este estudio con tinciones de inmunohistoquimica, para confirmacion diagnostica.
bueno el medico me señala que debe hacer quimioterapia,, pero no me ha dicho nada o no ha sido muy claro o yo no entiendo bien… Si alguno de UDS me puede explicar que nivel de gravedad tengo se los agracedere…